阿尔茨海默病 (AD) 病例数量不断增加,预计到 2050 年将达到 1.35 亿,这凸显了对有效治疗方法的迫切需求。累积的证据表明阿尔茨海默病患者的代谢机制受损,这种受损在痴呆症发作和认知功能退化前几十年就已经出现。新陈代谢减少是由线粒体功能障碍引起的,线粒体负责产生细胞中的大部分能量,但也参与细胞死亡、炎症和免疫反应。
尽管这种疾病与线粒体功能障碍有关,但目前还没有候选药物针对这一方面。内盖夫本古里安大学的研究人员提出了一种新的治疗方法,该方法针对线粒体守门人,电压依赖性阴离子通道 1 (VDAC1),它控制线粒体活动并控制细胞生死。
正如Translational Neurodegeneration杂志所报道的那样,新提出的目标和疗法在小鼠模型的多个参数上表现出显着改善。
VDAC1在线粒体介导的细胞死亡过程中起着至关重要的作用,这就是为什么Varda Shoshan-Barmatz教授领导的研究团队选择将他们的努力集中在阿尔茨海默病小鼠模型中的线粒体功能障碍作为目标进行治疗。
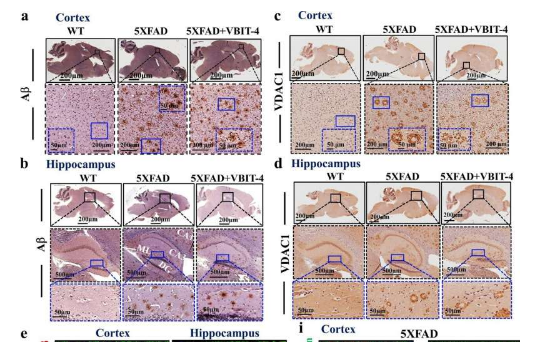
Shoshan-Barmatz 教授的研究表明,细胞中 VDAC1 蛋白数量的增加导致其组织成环状,具有死亡因子蛋白和线粒体 DNA 退出的大通道,导致细胞死亡和免疫反应, 分别。在心脏病、肠道疾病(克罗恩病)、自身免疫性疾病(狼疮)和其他疾病中发现 VDAC1 水平显着升高。在这里,研究人员表明,这种蛋白质在阿尔茨海默病小鼠模型的大脑中大量产生,并集中在斑块周围的神经细胞中,导致它们死亡。
Shoshan-Barmatz 教授开发了一种小分子 VBIT-4,它与 VDAC1 结合并防止与阿尔茨海默氏症相关的病理生理变化。VBIT-4 是一种可以穿过血脑屏障(BBB) 的分子,能够预防与阿尔茨海默病相关的病理生理变化,例如神经元细胞死亡、神经炎症和神经代谢功能障碍。此外,它还在星形胶质细胞和小胶质细胞中诱导神经保护表型,这些表型通常具有促炎性和神经毒性。
标签:
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!