慢性乙型肝炎病毒 (HBV) 感染可导致晚期肝病。HBV 感染人类已有 10,000 多年历史,通过协调病毒基因表达来建立持续感染。
人们普遍认为,HBV 不会直接导致感染的肝细胞致病;慢性肝炎和相关肝损伤的进展是由于病毒感染细胞与宿主免疫反应之间复杂的相互作用。然而,这一观点需要在病理生理学背景下重新审视。HBV 基础核心启动子 (BCP) 中自然发生的双重突变 C1766T/T1768A 与致命的暴发性肝炎有关,并导致 HBc 生成增加高达 15 倍。
在这项研究中,苏和他的同事建立了一个表达 BCP 突变 HBV 基因组的转基因小鼠模型。与之前对野生型病毒的研究不同,BCP 突变 HBV转基因小鼠表现出慢性肝损伤,最终导致肝硬化和肿瘤发展,随着年龄的增长。值得注意的是,激动剂抗 Fas 治疗即使在微不足道的剂量下也会在这些小鼠中诱发暴发性肝炎,这让人想起线粒体调节的死亡信号放大。
该研究发表在《科学公报》上。
BCP 突变的 HBV 转基因小鼠为了解慢性乙型肝炎的进展提供了有价值的模型。由于 BCP 突变体表现出 HBV 核心蛋白 (HBc) 表达显著增加,因此推测 HBc 积极参与肝细胞损伤。
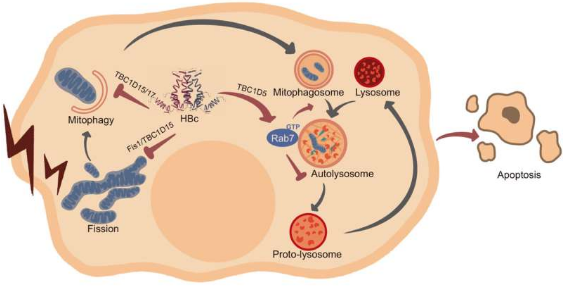
与此想法一致,作者发现 HBc 会干扰 Fis1 刺激的 Tre-2/Bub2/Cdc16 结构域家族成员 15 (TBC1D15) 的线粒体募集。HBc 还可以通过结合其保守的催化结构域来抑制多种 Rab GTPase 活化蛋白,包括 Rab7 特异性 TBC1D15 和 TBC1D5。
因此,在细胞受到线粒体压力时,HBc 会扰乱线粒体动力学并阻止受损线粒体的循环。此外,持续的 HBc 表达会通过 Rab7 过度活化导致溶酶体消耗,这进一步阻碍了晚期自噬并显著增加凋亡细胞死亡。
标签:
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!