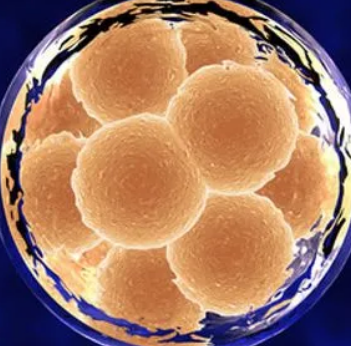
在人类胚胎发育的最早阶段,一小部分称为人类胚胎干细胞 (hESC) 的细胞协调生长和分化,最终形成高度特化的人类组织。作为多能细胞——体内每种细胞类型的祖细胞——hESC 是发育和再生生物学家的核心兴趣所在。许多驱动 hESC 功能的基因以前已经被确定,但揭示这些基因相关活动的强大工具直到最近才出现。布莱根妇女医院的研究人员和哈佛医学院使用全基因组遗传筛选来过度表达和灭活(“敲除”)hESC 中数以万计的基因。他们发现了同时控制多能性和细胞死亡(细胞凋亡)准备状态的关键网络,有助于确保胚胎发育的最佳条件。该研究的结果发表在基因与发育,提供了对癌症遗传学的新见解和再生医学研究的新方法。
“我们的方法使我们能够在人类基因组中创建几乎所有基因的‘图谱’,并确定其过度表达或亏损确实给人类发展的最根本的第一步,说:”主要作者卡米拉Naxerova,博士,曾任布莱根遗传学部Elledge 实验室的博士后研究员。“我们不是一个一个地观察基因,而是同时观察数以千计的基因改变,以确定它们如何影响胚胎干细胞的增殖,以及随后作为原材料的三个胚层的发育。用于人体组织。”
“阐明人类胚胎干细胞功能如何受遗传学控制对于我们理解发育生物学和再生医学至关重要,”共同通讯作者、布里格姆和英国皇家医学院的 Gregor Mendel 遗传学和医学教授 Stephen Elledge 博士说。“我们的研究提供了迄今为止最广泛的 hESC 基因功能检查。”
在进行他们的实验(包括敲除大约 18,000 个基因和过度表达 12,000 个基因)时,研究人员注意到 hESC 基因在控制多能性或分化能力方面发挥的独特作用。当研究人员删除这些众所周知的基因,其中包括OCT4和SOX2 时,干细胞出人意料地增加了它们对死亡的抵抗力,这表明在正常情况下,多能性调节因子也有助于细胞凋亡途径。研究人员假设,多能性和严格控制的细胞死亡之间的遗传联系有助于确保如果干细胞受损,它会在胚胎发育的早期被破坏,然后才能损害未来细胞和组织的功能。
这些相互关联的行为在称为 SAGA 复合体的多能性调节器中尤为明显。研究人员首次证明,在没有 SAGA 复合物的情况下,hESC 不太容易死亡。此外,它的缺失抑制了所有三个胚层(内胚层、中胚层和外胚层)的发育,证明了 SAGA 复合物在一系列 hESC 活动中的核心作用。最后,研究人员观察到,当它们在体细胞中过度表达或表达不足时,许多调节三个胚层形成的基因也是已知的癌症生长的因素。
除了提供有关癌症遗传基础的新视角外,该研究的高通量遗传筛查方法可能会为再生生物学的未来工作提供信息。
标签:
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!