由 Drs 领导的研究。路易斯安那州立大学健康新奥尔良神经科学中心和细胞生物学和解剖学、神经学和眼科的 Yuhai Zhao 和 Walter J Lukiw 首次报告了一条从肠道开始并以大脑中的强效促炎毒素结束的通路细胞有助于阿尔茨海默病 (AD) 的发展。他们还报告了一种简单的预防方法。结果发表在神经病学前沿。
研究人员发现的证据表明,一种含有非常有效的微生物产生的神经毒素(脂多糖或 LPS)的分子源自人类胃肠道 (GI) 中的革兰氏阴性细菌脆弱拟杆菌,它会产生一种称为 BF-LPS 的神经毒素。
“一般而言,LPS 可能是已知的最有效的微生物来源的促炎性神经毒性糖脂,”Lukiw 博士说。“许多实验室,包括我们自己的实验室,都在受阿尔茨海默病影响的人脑神经元中检测到不同形式的 LPS 。”
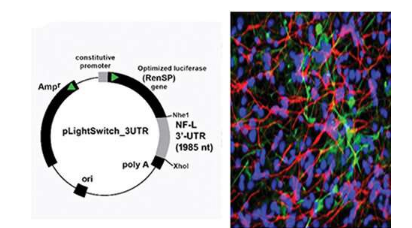
在这项研究中,研究人员详细介绍了 BF-LPS 从肠道到大脑的途径及其作用机制。BF-LPS 从胃肠道漏出,通过循环系统穿过血脑屏障,进入脑室。然后它会增加脑细胞的炎症并抑制神经元特异性神经丝光 (NF-L),这是一种支持细胞完整性的蛋白质。这种蛋白质的缺乏会导致进行性神经元细胞萎缩,并最终导致细胞死亡,正如在受 AD 影响的神经元中所观察到的那样。他们还报告说,摄入足够的膳食纤维可以阻止这一过程。
这种新描述的病理途径的新特征是三重的。AD 刺激途径开始于我们内部——在我们的胃肠道微生物群中——因此非常“本地化”并且在我们的一生中都很活跃。高效神经毒素 BF-LPS 是基于胃肠道的微生物代谢的天然副产品。微生物组中脆弱拟杆菌的丰度是神经毒素 BF-LPS 的来源,可以通过膳食纤维摄入来调节。
“换句话说,基于饮食的方法来平衡微生物组中的微生物可能是一种有吸引力的方法,可以改变 AD 相关微生物的产肠毒素形式的丰度、物种形成和复杂性,以及它们对高神经毒性微生物的病理排放的潜力——衍生的分泌物包括 BF-LPS 和其他形式的 LPS,”Lukiw 解释说。
研究人员得出结论,对胃肠道-中枢神经系统轴和胃肠道微生物组与阿尔茨海默病之间相互作用的更好理解具有相当大的潜力,可以在阿尔茨海默病和其他致命疾病的临床管理中产生新的诊断和治疗策略,进行性和年龄相关的神经退行性疾病。
标签:
免责声明:本文由用户上传,如有侵权请联系删除!