牛津大学领导的一项合作研究是英国 100,000 基因组计划的一部分,今天发表在《自然遗传学》上,该研究定义了最常见的血癌类型慢性淋巴细胞白血病 (CLL) 的五个新亚群,并将这些亚群与临床结果相关联.这种对患者进行风险分层的新方法可能会带来更加个性化的患者护理。
这是第一项分析整个癌症基因组而非靶向区域的所有相关 DNA 变化的研究,以对癌症患者进行分类并将这些亚组与临床结果联系起来。
领导这项研究的牛津大学肿瘤学系 Anna Schuh 教授说:“我们知道,癌症基本上是一种由个体一生中获得的 DNA 变化引起的疾病。我们目前使用的实验室工具预测患者是否可能对给定疗法产生反应通常只关注癌症 DNA 中的单一异常,并不能准确预测患者的临床结果。这就是为什么我们问了一个简单的问题:我们能否提高当前检测的精度通过一次查看癌症中所有获得的 DNA 变化?”
这项研究分析了485 名 CLL 患者的全基因组序列,这些患者参加了由利物浦大学和利兹大学领导的国家临床试验,为利物浦的英国 CLL 生物库提供样本,并同意将他们的样本用于 100,000 基因组计划由 Genomics England 运营。
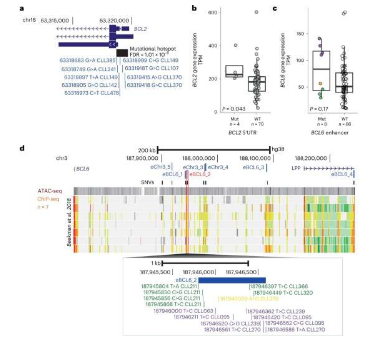
通过比较这些患者的癌症和健康组织的全基因组测序数据,该团队能够绘制已知和新发现的 DNA 变化、结构改变、癌症突变特征以及与整个基因组中的 CLL 相关的其他全局测量。他们确定了 186 种不同且反复出现的基因组改变,并使用这些改变定义了与不同临床结果相关的五个 CLL 基因组亚组。
在接受比本研究中包括的治疗范围更广的治疗(特别是靶向治疗)的患者中进行额外验证后,这些新的 CLL 基因组亚组可用于更好地指导治疗选择,以改善患者预后。
这项研究为全基因组分析在其他癌症类型中进行风险分层的常规临床应用铺平了道路。
该团队的分析还确定了 148 个新的假定 CLL 遗传驱动因素。未来对这些驱动因素的研究可能会揭示 CLL 起始和进展的新机制,并具有开发新疗法的潜力。
标签:
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!