帕金森病是一种神经退行性疾病,其特征是破坏特定的神经元群:多巴胺能神经元。这些神经元的退化阻止了控制特定肌肉运动的信号的传递,并导致震颤、不自主的肌肉收缩或这种病理特征的平衡问题。日内瓦大学 (UNIGE) 的一个团队使用果蝇作为研究模型,研究了这些多巴胺能神经元的破坏。科学家们在果蝇和老鼠身上发现了一种关键蛋白质,它对这种疾病具有保护作用,可能成为一种新的治疗靶点。这项工作可以在Nature Communications杂志上阅读。
除了涉及单个基因的罕见形式外,大多数帕金森病病例是由多种遗传和环境风险因素之间的相互作用引起的。然而,疾病发作的一个共同因素是多巴胺能神经元中的线粒体功能障碍。细胞内的这些小工厂负责产生能量,但也负责在细胞受损时激活细胞的自毁机制。
UNIGE 理学院遗传学与进化系教授 Emi Nagoshi 的实验室使用果蝇或果蝇来研究多巴胺能神经元退化的机制。她的团队对 Fer2 基因特别感兴趣,该基因的人类同源物编码一种蛋白质,该蛋白质控制许多其他基因的表达,其突变可能通过尚未完全了解的机制导致帕金森病。
在之前的一项研究中,这个科学团队证明了 Fer2 基因的突变会导致果蝇出现帕金森病样缺陷,包括运动开始的延迟。他们还观察到多巴胺能神经元线粒体形状的缺陷,类似于在帕金森病患者中观察到的缺陷。
保护神经元
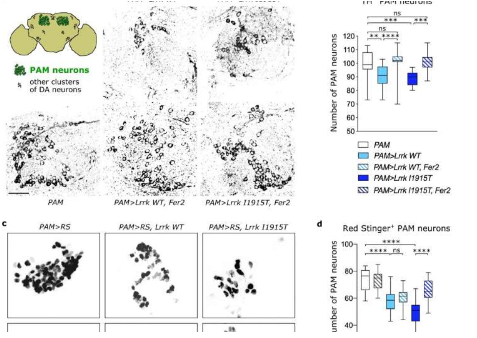
由于缺乏 Fer2 会导致类似帕金森病的病症,研究人员测试了是否——相反——细胞中 Fer2 含量的增加可能具有保护作用。当苍蝇暴露于自由基时,它们的细胞会经历氧化应激,从而导致多巴胺能神经元的退化。然而,科学家们能够观察到,如果果蝇过量产生 Fer2,氧化应激不再对果蝇产生任何有害影响,从而证实了其保护作用的假设。
“我们还确定了受 Fer2 调控的基因,这些基因主要参与线粒体功能。因此,这种关键蛋白似乎通过控制线粒体的结构及其功能,在对抗果蝇多巴胺能神经元的退化方面发挥着至关重要的作用, ” 遗传与进化系研究员、该研究的第一作者 Federico Miozzo 解释道。
新的治疗靶点
为了确定 Fer2 是否在哺乳动物中发挥相同作用,生物学家在小鼠多巴胺能神经元中创建了 Fer2 同源物的突变体。与苍蝇一样,他们观察到这些神经元的线粒体异常以及老年小鼠的运动缺陷。“我们目前正在测试 Fer2 同源物在小鼠中的保护作用,与在苍蝇中观察到的结果相似的结果将使我们能够为帕金森病患者考虑一个新的治疗靶点,”Nagoshi 总结道。
标签:
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!