加利福尼亚大学圣地亚哥分校医学院的研究人员发现了一种导致SAV-CoV-2(导致的)劫持人类细胞机制以钝化免疫反应,使其建立感染,复制并引起疾病的方法。 。
简而言之,该病毒的基因组被一种特殊的标记物标记了一种人类酶,该酶指示免疫系统停止运转,同时又增加了SARS-CoV-2用作“门把手”的表面蛋白的产量。进入细胞。
这项研究于2021年4月22日发表在《细胞报告》上,该研究为新的抗病毒免疫疗法奠定了基础-这些疗法通过增强患者的免疫系统而不是直接杀死病毒来发挥作用。
加州大学圣地亚哥分校医学院儿科遗传学系主任兼教授塔里克·拉纳(Tariq Rana)博士说:“使用宿主机同时进入隐身模式并进入更多细胞内,这种病毒非常聪明。”和摩尔斯癌症中心。“我们对病毒如何在体内建立自己的了解越多,我们就越有能力破坏它。”
在人类细胞中,基因(DNA)被转录为RNA,然后被翻译为蛋白质,即构成大多数细胞的分子。但这并不总是那么简单。细胞可以化学修饰RNA以影响蛋白质的产生。这些修饰之一是向腺苷中添加甲基,腺苷是组成RNA的构件之一。这种修饰被称为N6-甲基腺苷(m6A),在人类和其他生物(包括病毒)中很常见。
与人类相反,某些病毒的整个基因组,包括SARS-CoV-2,都是由RNA而不是DNA组成的。并没有携带将其翻译成蛋白质的机制,而是让人类细胞来完成这项工作。
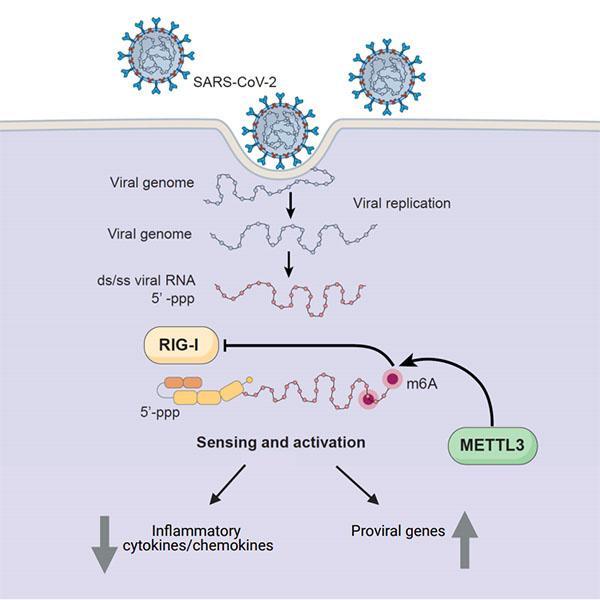
Rana和他的团队先前发现,m6A在HIV和Zika病毒感染中起着重要作用。在他们的最新研究中,研究人员发现人类酶METTL3添加了甲基,从而将m6A引入SARS-CoV-2的RNA中。这种修饰可以防止病毒的RNA触发称为细胞因子的炎症分子。令团队惊讶的是,METL3的活性还导致前病毒基因的表达增加-那些编码SARS-CoV-2复制和生存所需的蛋白质的基因,例如ACE2,该病毒可用于进入人类细胞的细胞表面受体。
拉娜说:“我们的细胞为什么能像这样帮助病毒,还有待观察。”
当研究小组在实验室中使用基因沉默或其他方法从细胞中去除METTL3时,他们看到了相反的结果-一种称为RIG1的促炎分子与病毒RNA结合,产生了更多的炎性细胞因子,并且抑制了促病毒基因。最终,抑制METTL3抑制了病毒复制。
标签: SARSCoV2
免责声明:本文由用户上传,如有侵权请联系删除!