来自,美国和英国的国际研究人员团队分析了组蛋白脱甲基酶KDM5A在多发性骨髓瘤(三大主要血液学癌症之一)中的功能,并阐明了其促进骨髓瘤细胞增殖的机制。他们还开发了一种新型的KDM5抑制剂,并表明它可以抑制骨髓瘤小鼠模型中的癌细胞生长。研究人员预计,将来会开发针对KDM5A的新疗法。
随着新治疗剂的引入,多发性骨髓瘤的预后每年都在改善,但仍无法治愈。需要进一步阐明该癌症的发病机理和开发治疗剂。包括多发性骨髓瘤在内的癌症的分子发病机理不仅与遗传变异而且与表观遗传学改变都密切相关。表观遗传调节因子KDM5家族蛋白在骨髓瘤细胞中高度表达,但其功能尚不清楚。
为了阐明KDM5家族蛋白在骨髓瘤细胞中的作用,熊本大学和达纳-法伯癌症研究所的研究人员使用基因操作来抑制KDM5在人骨髓瘤细胞系中的表达。他们发现,在KDM5家族成员中,特别是KDM5A对细胞增殖有很强的作用,促使他们分析其分子机制。他们还开发了一种新型KDM5抑制剂,并使用骨髓瘤患者细胞和骨髓瘤小鼠模型验证了其功效。
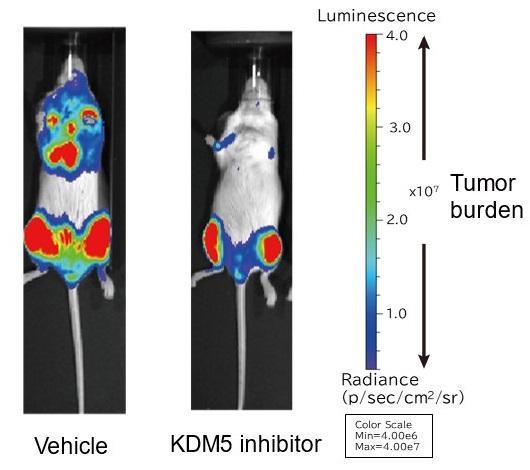
KDM5A表达的遗传抑制或KDM5的药理学抑制抑制了骨髓瘤细胞的生长。此外,通过使用将人类骨髓瘤细胞系移植到免疫缺陷小鼠中的骨髓瘤小鼠模型,研究人员证明了他们的KDM5抑制剂即使在体内也能抑制骨髓瘤细胞的生长。功能分析表明,KDM5A与MYC协同作用,MYC是骨髓瘤发生和发展的重要转录因子,可促进MYC目标基因的表达。尽管最初在MYC目标基因的转录起始位点附近观察到高水平的组蛋白甲基化(H3K4me3),但通过抑制KDM5A进一步提高了这种修饰水平。这表明过量的H3K4me3充当了转录的屏障,从而抑制了转录,这与以前的H3K4me3促进转录的理论相反。进一步的分析表明,KDM5A通过瞬时释放H3K4me3,帮助转录相关复合物从转录起始过渡到转录延伸。
这项研究提出了一种表观遗传调控的新模型,其中KDM5A在所需阶段将转录起始位点的组蛋白甲基化调节至最佳水平,从而促进MYC靶基因的转录并导致骨髓瘤细胞增殖。还表明KDM5抑制剂抑制骨髓瘤细胞的生长。
“我们的研究阐明了由组蛋白修饰调控介导的骨髓瘤细胞增殖的部分机制,并显示了靶向KDM5A的疗法的潜力,”主持这项研究的Hiroto Ohguchi副教授说。“还很明显,KDM5家族参与了其他癌的生长。迄今为止,KDM5抑制剂的问题在于它们的细胞膜通透性较弱,并且在细胞或体内均无效。该药物是基于这项研究中开发的KDM5抑制剂开发的,通过将其与常规治疗方法相结合,有望发展成为一种新的治疗策略,不仅可以治疗多发性骨髓瘤,还可以治疗多种其他类型的癌症。”
标签: 多发性骨髓瘤
免责声明:本文由用户上传,如有侵权请联系删除!