导读 由 HIF-1α 染色划定的缺氧区域表现出 E-钙粘蛋白丢失和波形蛋白和 EMT 介质 FOXC2 水平升高的焦点区域。与单独注射或与 HMLE
由 HIF-1α 染色划定的缺氧区域表现出 E-钙粘蛋白丢失和波形蛋白和 EMT 介质 FOXC2 水平升高的焦点区域。与单独注射或与 HMLE 载体细胞混合的 MCF-7 细胞相比,植入 MCF-7 细胞与过表达 EMT 诱导剂 Snail 的人乳腺上皮细胞共同混合,显着增强肿瘤生长和血管形成。
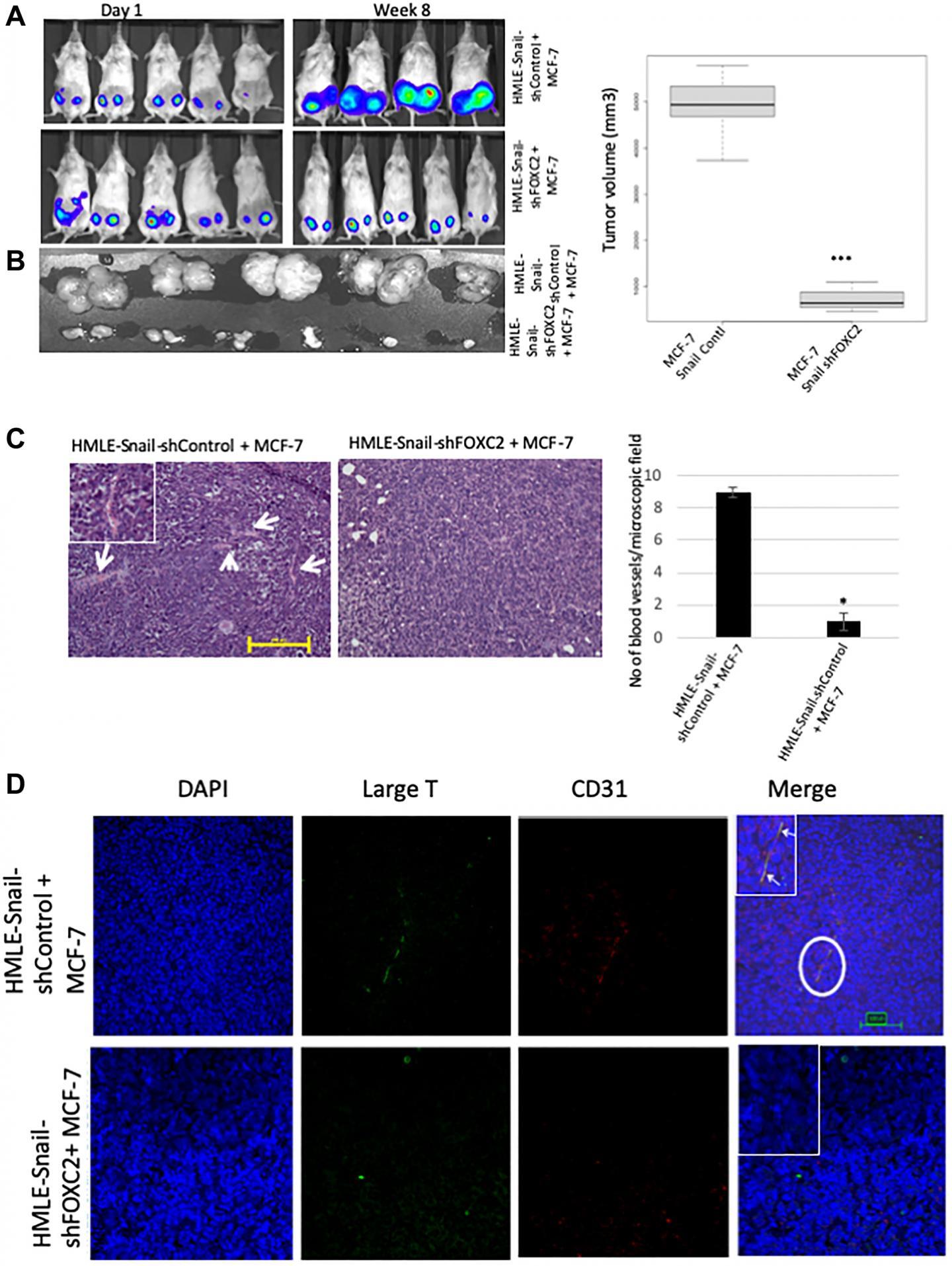
肿瘤内血管含有源自任一供体细胞类型的 CD31 阳性细胞。
FOXC2敲低消除了 HMLE-Snail 细胞对 MCF-7 肿瘤生长和血管化的增强作用,并损害了在内皮生长培养基中培养的间充质细胞的内皮转分化。
因此,经过 EMT 的细胞可以通过促进癌细胞的内皮转分化间接或直接通过获得内皮表型来促进肿瘤生长和新血管形成,FOXC2 在这些过程中起关键作用。
经历过 EMT 的细胞可以通过促进癌细胞的内皮转分化间接或直接通过获得内皮表型来促进肿瘤生长和新血管形成,FOXC2 在这些过程中起关键作用
得克萨斯大学 MD 安德森癌症中心和得克萨斯 A&M 大学的Tapasree Roy Sarkar 博士说:“血管生成是一种正常的生理过程,它需要通过重塑预先存在的脉管系统来发育新血管,由内皮细胞支持细胞萌芽、增殖和融合”
第四种机制——称为血管生成模拟——需要从头生成微血管,内衬嵌入丰富细胞外基质的高侵袭性肿瘤细胞,本质上模仿真正的血管内皮,尤其是缺乏内皮细胞标记物 CD31 和 CD34。
标签: 内皮细胞
免责声明:本文由用户上传,如有侵权请联系删除!