东京工业大学的科学家们开发了一种基于大规模分子动力学模拟的计算方法,可以使用超级计算机预测环肽的细胞膜渗透性。他们的协议显示出有希望的准确性,并可能成为设计和发现环肽药物的有用工具,这可以帮助我们在细胞内达到超出常规小分子药物或基于抗体的药物能力的新治疗靶点。
环肽药物作为传统小分子药物的有前途的替代品,引起了世界各地主要制药公司的关注。通过适当的设计,可以定制环肽以达到细胞内的特定目标,例如蛋白质-蛋白质相互作用,这超出了小分子的范围。不幸的是,众所周知,设计具有高细胞膜渗透性的环肽是非常困难的——也就是说,环肽可以很容易地扩散穿过界定细胞内部和外部的脂质双层。
为了解决这个瓶颈,中分子基于 IT 的药物发现实验室 (MIDL) 的科学家们一直在研究一种预测细胞膜渗透性的计算方法。MIDL成立于2017年9月,是东京工业大学(Tokyo Tech)超越院系界限的“研究计划”之一。在文部科学省(MEXT)区域创新生态系统建设计划的支持下,MIDL一直与川崎市合作,将发现中分子药物的框架产业化——环肽药物和核酸药物比常规小分子药物大但比抗体药物小——结合计算药物设计和化学合成技术。
在最近发表在《化学信息与建模杂志》上的一项研究中,Yutaka Akiyama 教授及其来自 MIDL 和东京理工大学的同事开发了一种使用分子动力学模拟预测环肽细胞膜渗透性的方案。这种模拟构成了一种广泛接受的计算方法,通过以短时间间隔顺序求解牛顿运动定律来预测和再现原子和分子的动力学。然而,即使是预测只有 8 个氨基酸的环肽的渗透性的单一模拟也需要花费大量的时间和资源。“我们的研究标志着首次对多达 156 种不同的环肽进行综合模拟,”Akiyama 教授强调说,“
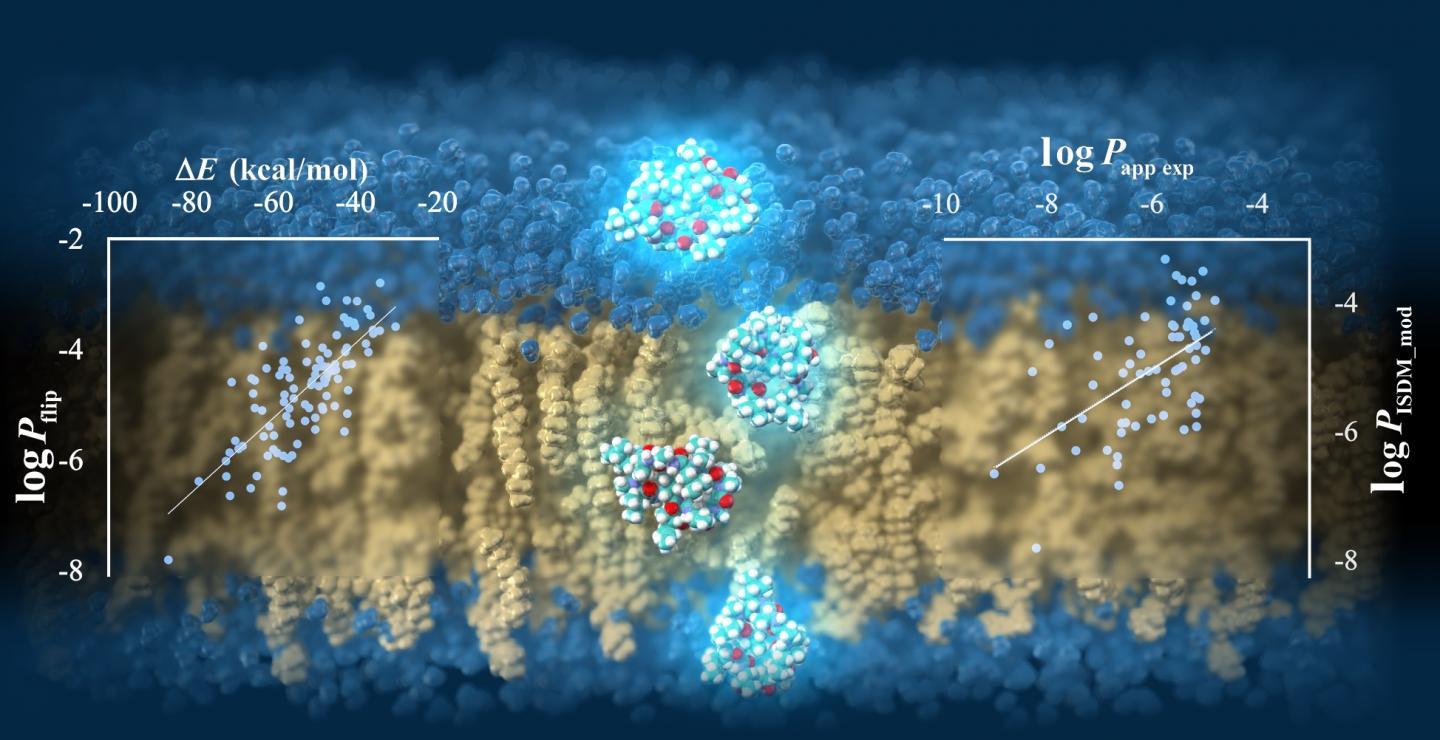
研究人员用实验得出的渗透率值验证了预测的渗透率值,并确认了在最佳条件下可接受的相关系数 R = 0.63,展示了他们协议的潜力。此外,在对从轨迹数据中获得的肽构象和能量值进行详细分析后,Akiyama 教授的团队发现,构成环肽的原子与周围介质,即脂质膜和水分子之间的静电相互作用强度,与膜渗透率值密切相关。模拟还揭示了肽通过根据周围环境改变其方向和构象来渗透膜的方式(图)。”我们的结果揭示了细胞膜通透性的机制,并为设计可以更有效地进入细胞的分子提供了指导。这将极大地促进下一代肽药物的开发,”该研究的第一作者 Masatake Sugita 教授评论道。
标签: TSUBAME超级计算机
免责声明:本文由用户上传,如有侵权请联系删除!