UT Southwestern 研究人员的新发现有助于更好地了解癌症最常见的突变遗传驱动因素之一如何传递导致疾病的信号。
该研究发表在Nature Structural & Molecular Biology 上,重点关注一个称为 RAS 的蛋白质家族,该家族在 20% 至 25% 的癌症中发生突变,尤其是在胰腺癌、结肠直肠癌和肺癌等致命癌症中。
“迫切需要一个开发 RAS 抑制剂策略的框架,因为最近批准的 RAS 抑制剂如索托拉西只对一种特定突变起作用,而许多其他 RAS 突变也会导致癌症,”医学博士、医学博士 Kenneth Westover说。,放射肿瘤学和生物化学副教授,德克萨斯州西南部哈罗德 C.西蒙斯综合癌症中心化学和癌症研究项目成员,以及该研究的作者。“这项工作为开发新的靶向 RAS 抑制剂以解决致命癌症(如胰腺癌和结肠癌)的主要驱动因素奠定了基础。”
从 2012 年开始,Westover 博士的实验室与 Dana-Farber 癌症研究所合作开发与特定 RAS 突变体结合的药物,其中 RAS 蛋白第 12 位的甘氨酸氨基酸变为半胱氨酸,即所谓的 KRAS G12C .
“半胱氨酸是一种独特的氨基酸,它使我们能够使用特殊的化学物质不可逆地附着药物。其他主要的癌症相关 RAS 突变并没有给我们同样的立足点,“韦斯托弗博士说。
他的实验室的工作帮助推动了该领域的发展,该领域在 5 月份获得了一种 KRAS G12C 抑制剂索托拉西的批准。广泛预期类似药物阿达格拉西的批准。
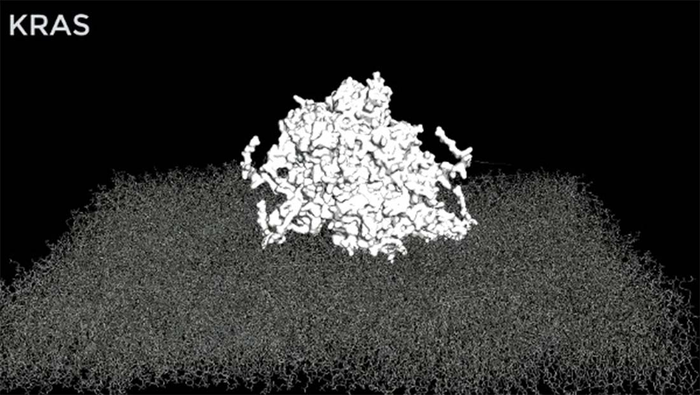
在最新的研究中,Westover 实验室试图了解致癌 RAS 突变体如何将不适当的信号从细胞表面传递到细胞核。作为机制的一部分,大蛋白质簇的形成是已知的,但簇的结构是未知的。Westover 博士及其合作者使用计算机模拟得出 RAS 组件的原子结构模型,并使用生物系统验证该模型。
“这种结构模型现在可供更广泛的 RAS 研究界使用。我们希望它能让研究人员测试关于 RAS 如何在正常生理学中起作用的新想法,以及针对致癌 RAS 突变的新策略,”西蒙斯癌症中心主任、医学博士 Carlos L. Arteaga说。
标签:
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!