中国上海复旦大学和中国科学院的研究人员进行了全脑基因组编辑,旨在纠正与小鼠自闭症谱系障碍(ASD)相关的单碱基突变。
在《自然神经科学》杂志上发表的一篇论文《全脑体内碱基编辑逆转了Mef2c 突变小鼠的行为变化》中,该团队详细介绍了他们在应用体内基因编辑方面的革命性进展,对临床神经科学具有重要意义。
该研究重点关注 MEF2C 基因内的单碱基突变,该基因与人类 ASD 相关。MEF2C 在特定大脑区域(皮质、海马、杏仁核)高度表达,在神经发育和突触可塑性中发挥着至关重要的作用。
MEF2C 基因突变会导致自闭症谱系障碍 (ASD),因为改变的基因会影响 MEF2C 蛋白质稳定性,导致蛋白质降解加速。由于参与神经元结构的关键蛋白质受损,神经元形态异常,导致发育缺陷,如智力障碍、缺乏言语和重复行为。
为了改变突变基因的配置,该团队开发了一种名为 AeCBE 系统(载脂蛋白 B mRNA 编辑酶,催化多肽嵌入胞嘧啶碱基编辑器)的碱基编辑系统,将 C·G 碱基对转换为 T·A 碱基对,而不会导致突变。双链 DNA 断裂。通过不允许双链断裂,该方法减少了插入缺失、意外添加或删除的机会。
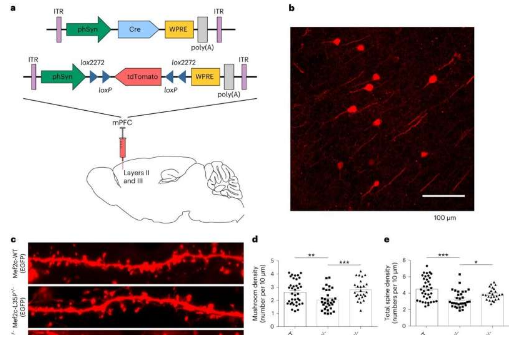
在实验中,携带 Mef2cL35P 突变的小鼠表现出模仿 ASD 特征的行为异常,如多动、重复行为和社交异常。通过跨越血脑屏障的腺相关病毒注射 AeCBE 成功纠正了小鼠大脑中的突变,恢复了各个大脑区域的 Mef2c 蛋白水平并逆转了行为异常。
这些发现为治疗由单基因突变引起的遗传性脑部疾病的潜在治疗方法提供了有希望的结果。该方法在活体小鼠身上的成功凸显了其在解决人类遗传性神经发育障碍方面的临床意义。
标签:
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!