筑波-在其他情况下,动脉粥样硬化和长期高血压会导致血管受伤。结果,血管可能会经历称为重塑的过程,从而使血管壁变厚并引起阻塞(称为阻塞)。在一项新的研究中,筑波大学的研究人员发现了主要存在于血管最外层的以血小板衍生的生长因子受体α(PDGFRa +)标记的细胞如何促进其重构。
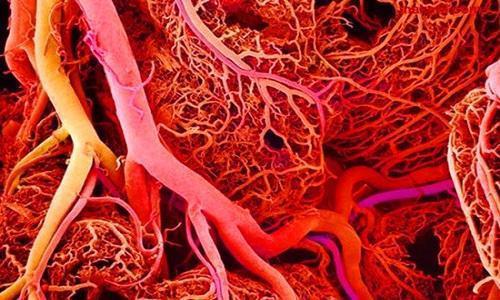
血管由三层组成,每一层在血管的功能和稳定性中起着独特的作用:最内层(内膜)衬有调节血液与组织之间交换作用的内皮细胞。中间层(介质)由调节血管张力的平滑肌细胞组成;最外层(外膜)包含各种细胞类型和结缔组织,可为血管提供结构完整性和稳定性。内膜对诸如动脉粥样硬化和高血压之类的病理状况高度敏感,但对由于支架植入引起的血管阻塞也高度敏感(也称为支架内再狭窄)。当内膜受损时,血管会发生重塑,从而使培养基中的平滑肌细胞繁殖并导致血管壁阻塞。
“新内膜形成是血管疾病和支架植入的主要并发症,”研究助理木村贤一教授说。“由于它们会影响患者的整体发病率和死亡率,因此了解导致新内膜形成的机制很重要,因此我们可以为患者提供治疗方法。过去,人们对培养基在新内膜形成中的作用进行了深入研究。因此,在这项研究中,我们想了解外膜细胞如何对其作出贡献。”
为了实现他们的目标,研究人员使用谱系追踪并用荧光蛋白标记了小鼠的PDGFRa +细胞。通过这样做,他们能够随着时间的推移识别和跟踪细胞群体及其后代。为了了解PDGFRa +细胞如何促进新内膜的形成,研究人员对小鼠的血管施加了三种不同类型的损伤:颈动脉结扎(绑在颈部的主要血管),剥脱术(使用金属丝损伤血管)内)和压力超负荷(系主动脉以增加由主动脉引起的血管中的血压)。
有趣的是,研究人员发现PDGFRa +细胞的反应根据损伤的类型而有所不同。尽管这些细胞在颈内动脉结扎后缓慢地分布在新内膜并发展为不成熟的血管肌细胞,但在剥脱性损伤的情况下,这一过程得以加速,PDGFRa +细胞则发展为成熟的血管平滑肌细胞。此外,在压力超负荷损伤后,PDGFRa +细胞在外膜中增殖并在那里产生结缔组织。
Hiromi Yanagisawa教授说:“这些惊人的结果表明PDGFRa +细胞如何表现出对血管损伤的背景依赖性反应。我们希望我们的发现可以为受新内膜形成和血管阻塞影响的患者提供新的治疗途径。”
标签: 血管损伤
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!