从环境中获取能量和营养——即进食——是一项非常重要的功能,数亿年来,它一直通过复杂的机制进行调节。其中一些机制现在才开始被解开。西班牙国家癌症研究中心 (CNIO) 的一个小组发现了他们的一个关键组成部分——一种控制生物体适应低细胞营养水平能力的开关。
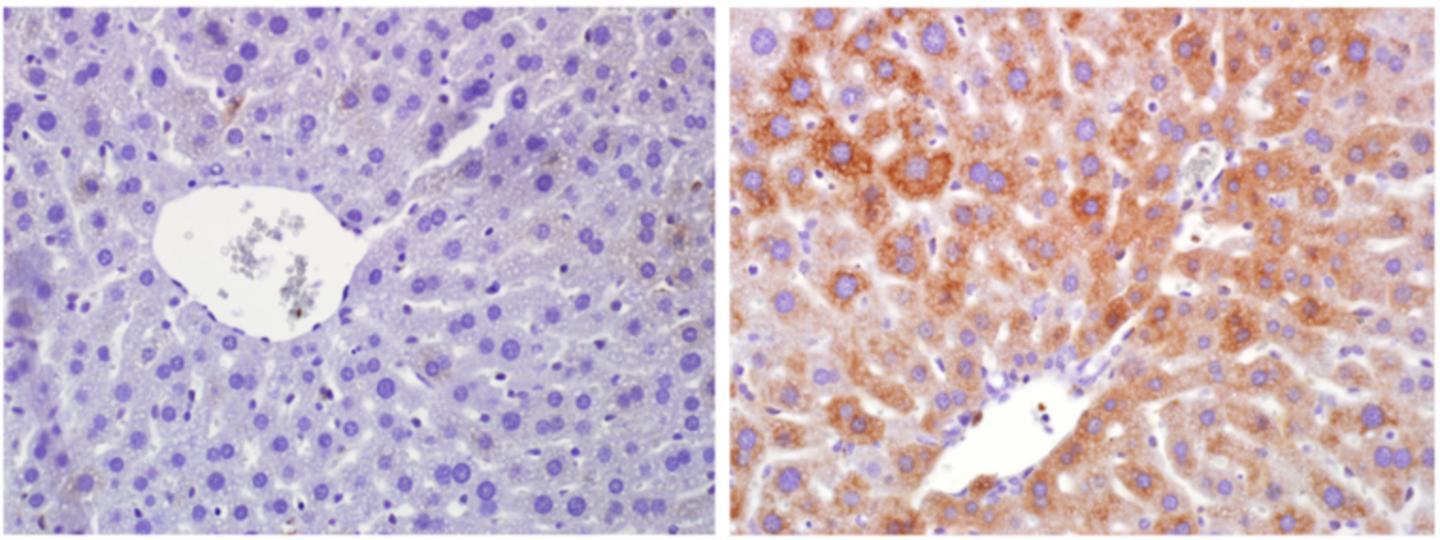
所涉及的蛋白质是 RagA,它是 mTOR 分子途径的一部分,其在代谢活动调节中的重要性几十年来一直为人所知。CNIO 研究人员发现,如果 RagA 持续激活,细胞不会知道没有足够的营养,因此会继续使用能量,就好像营养充足一样。
该研究本周发表在《自然通讯》上。通讯作者为 CNIO 代谢与细胞信号组组长 Alejo Efeyan,Celia de la Calle 为第一作者。
“今天,营养物质总是很丰富,”Efeyan 说,“但我们进化的条件却大不相同。”“我们的机体适应进食-禁食周期,我们的细胞准备对它们做出反应。我们发现 RagA 激活是我们适应禁食条件的关键”。
RagA 分子通路的重要性与在营养中起关键作用的其他成分(如胰岛素)的重要性不相上下。然而,RagA 是在不久前发现的,对其在代谢调节中的作用知之甚少。了解 Rag 蛋白在细胞中的运作方式可以让我们找到对抗肥胖和肥胖相关疾病(如脂肪肝或癌症)的新策略。
“适应营养水平的波动是所有生物体的基础,”Efeyan 解释说。“这是一种古老的分子途径,实际上比胰岛素更古老。甚至在酵母中也发现了它。尽管如此,人们对它如何影响正常生理机能以及它的活性如何在肥胖和肥胖相关条件下失调知之甚少。”
“保存模式”开启
在健康的生物体中,RagA 检测到低营养水平并相应地关闭,细胞代谢启用“节能模式”。然后,有机体变得更加“节俭”,使用营养丰富时储存的资源。
当 RagA 被激活时,小鼠“继续使用能量;它们不会将新陈代谢调整到正常的进食-禁食周期。它们的细胞‘相信’营养一直很丰富,并且不会节省能量,”第一作者 Celia de la Calle 说的研究。
CNIO 代谢和细胞信号传导组的研究人员此前已经证明了该系统的重要性。使用永久激活 RagA 的小鼠胚胎,他们表明,当营养物质不再通过胎盘输送时,动物无法适应出生时的营养缺乏。
标签: 禁食条件
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!