药物性肝损伤 (DILI) 是临床前安全性减员和上市后停药的主要原因。药物诱导的线粒体毒性已被证明在各种形式的 DILI 中发挥重要作用,尤其是在特异质肝损伤中。在这项研究中,作者检查了提交给食品和药物管理局 (FDA) 不良事件报告系统 (FAERS) 的肝损伤报告,这些报告与非线粒体毒性机制相比,通过线粒体机制与肝毒性相关的药物。
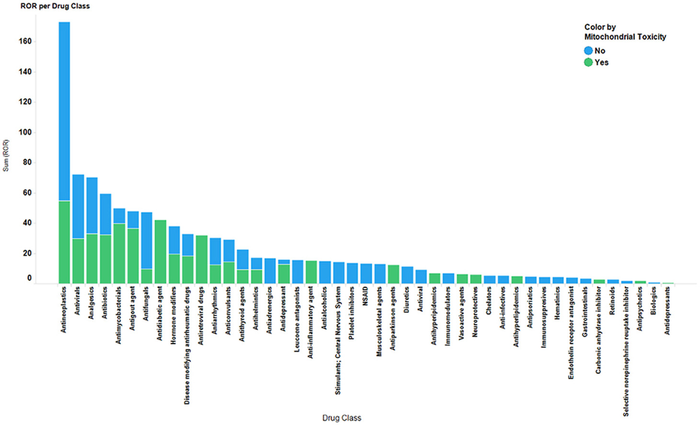
在组水平和个体药物水平上确定肝毒性的频率。报告优势比 (ROR) 被计算为效果的衡量标准。在两个 DILI 组之间,与非线粒体毒性机制相关的药物相比,涉及线粒体毒性机制的 DILI 报告的几率高 1.43(95% CI 1.42–1.45;P < 0.0001)倍。
抗肿瘤、抗病毒、镇痛、抗生素和抗分枝杆菌药物是 ROR 值最高的前五类药物。尽管 ROR 值最高的前 20 种药物包括具有线粒体和非线粒体损伤机制的药物,但前 4 种药物(ROR 值 > 18:苯溴马隆、曲格列酮、异烟肼、利福平)与线粒体毒性机制有关。还检查了 DILI 风险的主要人口统计学影响。
与非线粒体机制 [48 ± 19.53 (SD)] 相比,与线粒体毒性机制相关的药物报告中,患者的平均年龄更高 [56.1 ± 18.33 (SD)] (P < 0.0001),表明年龄可能通过线粒体毒性机制在对 DILI 的易感性中起作用。单变量逻辑回归分析显示,与涉及年龄小于 65 岁患者的报告相比,肝损伤报告与老年患者年龄相关的可能性高 2.2(优势比:2.2,95% CI 2.12-2.26)倍。
与男性相比,女性患者成为与线粒体毒性机制相关的药物肝损伤报告的受试者的可能性要低 37%(优势比:0.63,95% CI 0.61–0.64)。
鉴于与线粒体毒性机制相关的药物中严重肝损伤报告的比例较高,当药物设计替代方案、更具临床相关性的动物模型和更好的临床生物标志物可能提供时,必须了解药物在临床前药物开发过程中是否会导致线粒体毒性将药物诱导的线粒体毒性风险评估从动物更好地转化为人类。作者在这项研究中的发现与线粒体毒性机制是 DILI 的一个重要原因一致,这应该在具有稳健设计的真实世界研究中进一步研究。
标签:
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!