基因疗法以两种不同的方式治疗2种罕见的儿童疾病
2021年7 月 13 日——两项新研究指出了有效利用基因疗法来治疗致命的儿童遗传疾病。第一项研究使用直接基因疗法输注来治疗罕见的神经发育障碍,而第二项研究使用小鼠模型中的产前碱基编辑作为治疗遗传疾病的概念证明。这些截然不同的方法显示了基因治疗对多种破坏性疾病的前景。
基因治疗一号:通过病毒载体的直接DDC基因治疗
芳香族 L-氨基酸脱羧酶 (AADC) 缺乏症是一种罕见的神经发育障碍,其特征是多巴胺合成血清素不足。该缺陷仅影响全球 135 名儿童,是由 DOPA 脱羧酶 ( DDC ) 基因突变引起的,导致 AADC 酶功能失调。它会导致至少 70% 的患者出现身体和发育问题,包括智力障碍。
由俄亥俄州立大学韦克斯纳医学中心和俄亥俄州立大学医学院的研究人员领导的一项早期临床试验对 7 名 4-9 岁的 AADC 缺乏症儿童应用了直接基因疗法(用功能基因替代基因)。研究结果于 7 月 12 日发表在Nature Communications上。
校正后的基因(人 AADC 互补 DNA;hAADC)被包装到腺相关病毒血清型 2 (AAV2) 载体中。将 AAV2-hAADC 直接输注到中脑的两个区域。这些区域的多巴胺能神经元将分支投射到大脑的其他区域。因此,病毒载体的轴突运输能够沿着受基因突变影响的脑回路传播治疗基因。
直接基因疗法通过输液导管注入受试者大脑的特定区域。然后,研究人员使用实时磁共振成像 (MRI) 来确认载体传递。
“实际上,我们正在做的是向细胞引入不同的代码,”俄亥俄州立韦克斯纳医学中心神经病学研究所神经外科肿瘤学主任詹姆斯·埃尔德博士在一份声明中说。“而且我们正在现场观看整个过程。因此,我们不断重复核磁共振成像,我们可以看到所需细胞核内的输液开花。”
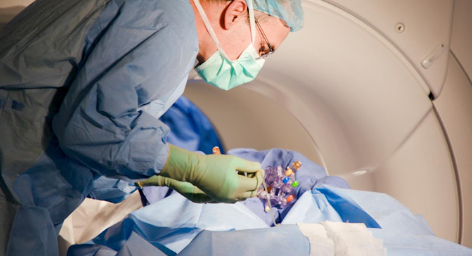
James Elder 博士在俄亥俄州立大学韦克斯纳医学中心进行基因治疗脑输注。.
James Elder 博士在俄亥俄州立大学韦克斯纳医学中心进行基因治疗脑输注。图片由俄亥俄州立大学韦克斯纳医学中心提供。
所有七名试验对象在临床功能和多巴胺产生方面都表现出可测量的改善,这表明生理区域(中脑)中 AADC 活性的恢复可以逆转在原发性 AADC 缺乏症中观察到的病理表型。
“值得注意的是,这些发作是基因治疗手术后消失的第一个症状,它们永远不会复发,”合著者、俄亥俄州立大学医学院神经外科教授 Krystof Bankiewicz 博士说。“在接下来的几个月里,许多患者经历了改变生活的改善。他们不仅开始大笑,心情也有所改善,而且许多人能够开始说话甚至走路。他们正在弥补他们在异常发育过程中失去的时间.”
该团队认为,该试验的方法和结果为治疗其他神经退行性疾病(如帕金森病和阿尔茨海默病)提供了框架。
基因治疗之二:产前碱基编辑
Hurler 综合征,也称为 I 型粘多糖贮积症 (MPS-IH),是一种溶酶体贮积病,影响全球约 100,000 名婴儿。这种疾病是由单个 DNA 碱基突变引起的,其中腺嘌呤取代了鸟嘌呤。该疾病在 6 个月以下的儿童中出现,表现为肝脾肿大、腹壁疝、肌肉骨骼异常、视网膜和神经认知退化以及心脏病。如果不及时治疗,患者可能会在 5 到 10 岁时死于心肺并发症。
目前对儿童的产后治疗包括终身免疫原性酶替代疗法和造血干细胞移植。产后全身基因治疗策略目前也在研究中,但仍然存在效率低下和安全问题。相比之下,CRISPR 碱基编辑可能提供一种潜在的安全和更有效的解决方案。
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
【关羽骑赤兔包公铡太师打一生肖】在中国传统文化中,历史人物、典故与生肖文化常常交织在一起,形成许多有趣...浏览全文>>
-
【关羽连招技巧】在《王者荣耀》中,关羽是一位非常具有操作性的英雄,拥有高机动性和强大的控制能力。掌握他...浏览全文>>
-
【关羽历史上是怎么死的】关羽,字云长,是三国时期蜀汉的重要将领,以忠义、勇猛著称。他在《三国演义》中被...浏览全文>>
-
【关羽和刘备的马分别叫什么】在中国古代历史与文学作品中,三国时期的人物形象深入人心,尤其是关羽、刘备等...浏览全文>>
-
【关羽的媳妇】在历史与文学的交汇中,关羽作为三国时期的重要人物,其形象深入人心。然而,关于他的家庭生活...浏览全文>>
-
【关羽的青龙偃月刀现在在哪里】在中国古代历史和文学中,关羽是一位极具传奇色彩的人物,他所使用的“青龙偃...浏览全文>>
-
【关羽的青龙偃月刀多重】在中国古代文学和民间传说中,关羽是一位极具传奇色彩的英雄人物,他的形象不仅体现...浏览全文>>
-
【关于中秋节的英语手抄报】中秋节是中国传统节日之一,每年农历八月十五庆祝。它不仅是家人团聚的日子,也是...浏览全文>>
-
【关于中秋节的小故事】中秋节是中国传统节日之一,承载着丰富的文化内涵和深厚的情感寄托。自古以来,人们在...浏览全文>>
-
【关于中秋节的文化含义】中秋节,是中国传统节日中最具代表性的节日之一,通常在农历八月十五这一天庆祝。它...浏览全文>>
