高级别浆液性癌是最具侵袭性的卵巢癌形式,占晚期病例的大多数。与该疾病相关的不良结果强调需要更有效的治疗方法。由芝加哥大学医学综合癌症中心主任、医学博士、医学博士 Kunle Odunsi 领导的一个研究小组发现了新的代谢机制,这些机制有助于卵巢癌如何逃避免疫攻击,以及联合疗法如何利用这些途径正如 2022 年 3 月 16 日发表在《科学转化医学》上的一篇论文中所报道的那样,改善卵巢癌的治疗。
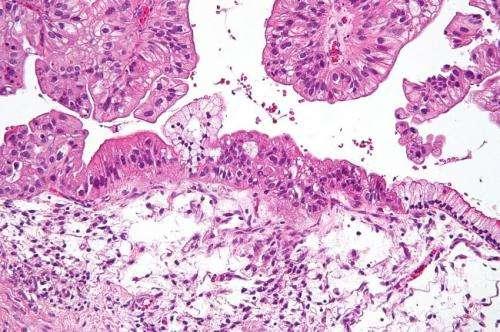
在过去的几年里,来自芝加哥大学、罗斯威尔帕克综合癌症中心和其他领先机构的研究人员联手解决了阻碍卵巢癌治疗取得突破的最紧迫问题之一——为什么卵巢癌的免疫治疗经常失败?更具体地说,他们探索了导致肿瘤能够逃避免疫系统破坏的潜在机制。
研究人员专注于靶向一种称为吲哚胺 2,3-双加氧酶 1 (IDO1) 的酶,该酶负责降解氨基酸色氨酸,以产生可以抑制肿瘤环境中抗癌免疫细胞(T细胞) 的分解产物。因为肿瘤已经意识到 T 细胞的生存严重依赖色氨酸,所以肿瘤会产生大量的 IDO1 以剥夺 T 细胞的色氨酸。先前的研究表明,用一种被称为 epacadostat (EPA) 的药物来靶向 IDO1 通路,可以阻断肿瘤关闭的 T 细胞。矛盾的是,IDO1 阻断联合免疫疗法在临床试验中显示出有限的成功,表明在 IDO1 生物学知识和阻断它的后果方面存在差距。
为了更好地了解卵巢癌是如何逃避免疫攻击的,研究小组想了解当 IDO1 被阻断时,肿瘤微环境(TME) ——周围支持肿瘤生长的正常细胞、分子和血管——究竟发生了什么。他们的搜索始于诊所,在那里他们收集了新诊断的晚期卵巢癌患者的组织样本,这些患者没有接受过手术或化疗。在患者接受为期两周的 EPA 治疗和切除肿瘤的手术后,他们再次收集样本。
标签:
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!