根据《自然通讯》发表的一项研究,一种能够结合mRNA并调节基因表达的新分子技术可能为治疗由单倍体不足或缺乏一个功能基因拷贝引起的疾病提供新途径。
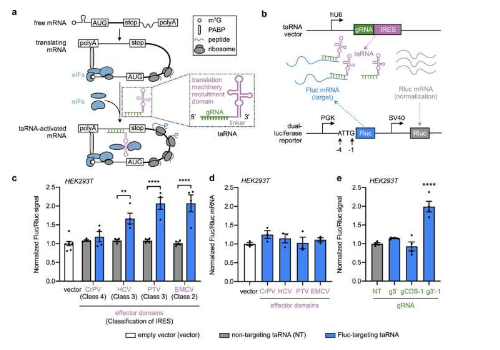
信使RNA(mRNA)包含DNA产生蛋白质的指令。许多疾病,包括癌症和许多遗传性疾病,都是由基因表达不足和蛋白质表达不足引起的,但很少有策略可以在分子水平上纠正这种失调。
这项新技术被称为“翻译激活RNA”(taRNA),由小分子组成主席AlfredL.GeorgeJr.医学博士和阿尔弗雷德·牛顿·理查兹(AlfredNewtonRichards)表示,这项组成,可附着在特定的mRNA分子上,从而直接控制它们翻译成蛋白质。药理学教授和该研究的合著者。
“这项技术为一种在蛋白质水平上增强基因表达的新方法打开了大门。敲低基因的方法有很多,但上调基因并从基因拷贝中产生更多蛋白质的方法却很少。该基因不会因突变而失效,”乔治说,他也是药物基因组学中心的主任。
这项研究是一项合作成果乔治和芝加哥大学化学教授布莱恩·迪金森博士(该论文的资深作者)之间的
在这项研究中,研究人员将RNA分子内的序列片段组合起来,创建了能够靶向PTEN(一种已知可作为有效肿瘤抑制剂的mRNA)和ABCA7(一种经常被发现在阿尔茨海默病患者中存在缺陷的mRNA)的taRNA。将taRNA注入培养的人类细胞后,研究人员发现两种mRNA的水平均有所增加。
然后,研究人员在侵袭性三阴性乳腺癌人类样本中对mRNA进行编程,使其与PTEN和CDKN1A(另一种与肿瘤抑制相关的基因)结合。研究表明,注射taRNA后,肿瘤生长减慢了一半。
George和他的合作者随后利用taRNA刺激人类神经元中SYNGAP1的产生。SYNGAP1是突触活动的主要调节因子,出生时仅具有该基因一个功能副本的儿童会患有癫痫症和神经发育严重受损。
根据这项研究,乔治实验室中接受taRNA的患者来源的诱导多能干细胞产生的人类神经元显示SYNGAP1蛋白恢复到正常水平。
乔治说,这项研究的结果为治疗由基因和蛋白质表达不足引起的各种疾病提供了一种有前途的新策略。
“这种方法在人类神经元中发挥作用的事实非常令人兴奋,”乔治说。“有许多技术在实验室的人工系统中有效,但在人体细胞中效果不佳。人类神经元尤其具有挑战性。”
乔治说,这项研究是机构合作推动新发现的一个很好的例子。
“西北大学的教师投入了大量精力,从患有罕见神经遗传和神经发育障碍(例如SYNGAP1相关智力障碍)的儿童中开发细胞系。这种细胞资源是测试新治疗策略的金矿,就像本文中介绍的那样,“乔治说。
“这项研究是芝加哥机构之间以及化学生物学家和我的实验室之间合作的一个很好的例子,该实验室利用疾病的干细胞模型研究人类疾病。”
标签:
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!