内吞作用和循环控制真核细胞对各种物质的吸收和回收。哺乳动物细胞已经发展出几种循环途径,包括研究相对广泛的“快速”和“慢速”管泡循环途径。然而,除了典型的“快速”和“慢速”循环途径之外的内吞循环途径仍然很大程度上未知。
中国科学院遗传与发育生物学研究所何康民博士后研究组最近发现了一种新的具有“吻后逃逸”膜融合的内吞回收机制,科学家将这一机制命名为网格蛋白相关快速内体回收途径(CARP)。
这种新颖的内吞回收途径采用了一组独特的分子机制来生成回收载体并促进意外的吻合-跑动膜融合。
这项研究题为“网格蛋白相关载体通过亲吻和逃跑机制实现回收”,于2024年9月19日发表在《自然细胞生物学》上。
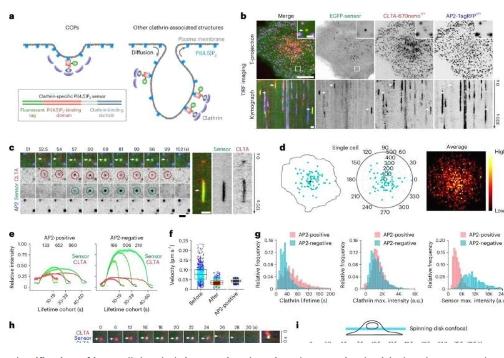
通过利用一种可选择性识别含有PI(4,5)P2的网格蛋白相关结构的“巧合检测”脂质生物传感器,研究人员发现了一群脂质传感器阳性但AP2阴性的网格蛋白相关结构,它们会暂时访问质膜。
利用先进的3D成像和超分辨率成像技术,发现这些结构是细胞内网格蛋白/AP1相关载体。
“一个引人注目的发现是,这些网格蛋白/AP1相关的回收载体可以部分与质膜融合,随后被回收和释放,”何康敏说。
为了表征网格蛋白相关回收载体的分子组成和特性,何教授团队进行了基于TIRF显微镜的成像筛选,确定了在网格蛋白相关回收载体的生成、接近、融合和回收的各个阶段招募的一系列蛋白质。
此外,他们证明这些载体是由缺乏检索复合物的早期内体子域产生的。
通过追踪GPCR家族中激动剂刺激的β2肾上腺素受体和受体酪氨酸激酶中的表皮生长因子受体的内吞循环,研究人员发现,这些网格蛋白相关的回收载体可以介导信号受体快速循环回质膜。
标签:
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!